重點快速看
前言
衛生福利部食品藥物管理署於 2019 年 7 月 1 日起施行化粧品衛生安全管理法,並同步公告《化粧品產品資訊檔案管理辦法》及「應建立產品資訊檔案之化粧品種類及實施日期」,以推行化粧品 PIF 建置制度,與全球化粧品管理接軌。
化粧品 PIF,英文全名 Product Information File,即產品資訊檔案,是業者在產品上市前必須建立並保存的一份完整技術文件,用以證明產品的安全性、品質與合法性,內容涵蓋配方、製程、安全性評估等,並由具備資格的專業人員簽署,是產品合法在台販售的必備「產品履歷表」。
化粧品 PIF 檔案之相關要求
所訂定之應建立產品資訊檔案之化粧品種類及實施日期在 2024 年 7 月 1 日即生效,只是依產品類別實施日期有所不同:
一、添加特定成分之化粧品,或具有防曬、染髮、燙髮、止汗制臭或含過氧化物之牙齒美白用途化粧品:2024 年 7 月 1 日實施。
二、嬰兒用、唇用、眼部用與非藥用牙膏、漱口水之化粧品:2025 年 7 月 1 日實施。
三、一般化粧品:2026 年 7 月 1 日實施。
依據化粧品產品資訊檔案管理辦法第三條,PIF 應以中文或英文建立下列資料:
1. 產品基本資料:產品名稱、產品類別、劑型、用途、製造廠名稱與地址及產品製造或輸入業者資訊。
2. 完成產品登錄之證明文件。
3. 全成分名稱及其各別含量。
4. 產品標籤、仿單、外包裝或容器。
5. 製造場所符合化粧品優良製造準則之證明文件或聲明書。
6. 製造方法、流程。
7. 使用方法、部位、用量、頻率及族群。
8. 產品使用不良反應資料。
9. 產品及各別成分之物理及化學特性。
10. 成分之毒理資料。
11. 產品安定性試驗報告。
12. 微生物檢測報告。
13. 防腐效能試驗報告。
14. 功能評估佐證資料。
15. 與產品接觸之包裝材質資料。
16. 產品安全資料:
1)經安全資料簽署人員簽名並載明日期之安全性評估結論與建議。
2)安全資料簽署人員符合相關能力資格規定之證明文件。
針對所需資料之其中三項:微生物檢測報告、防腐效能試驗報告及產品安定性試驗報告進行詳細介紹。
一、微生物檢測報告
依據衛授食字第 1101606101 號化粧品微生物容許量基準表,化粧品需符合下列規定:

因此,若業者本身無自主檢驗能力,則建議需送驗五項微生物套組:生菌數、大腸桿菌、綠膿桿菌、金黃色葡萄球菌及白色念珠菌,確保產品符合規範又滿足 PIF 所需資料。
二、防腐效能試驗報告
為了測試化粧品在使用過程中,防腐系統之有效性(抑菌效果),簡單來說,就是在產品中接種若干種類、一定數量的微生物,並定期檢測樣品中微生物的數量,觀察其數量是否有逐漸下降,若有則表示產品具有良好防腐效果。
防腐效能試驗所採取的檢測方法,可參考我國公告之化粧品防腐效能試驗指引或其他國際間之標準方法,以我國公布的指引為例,範例如下表(表格中數據皆為舉例)。
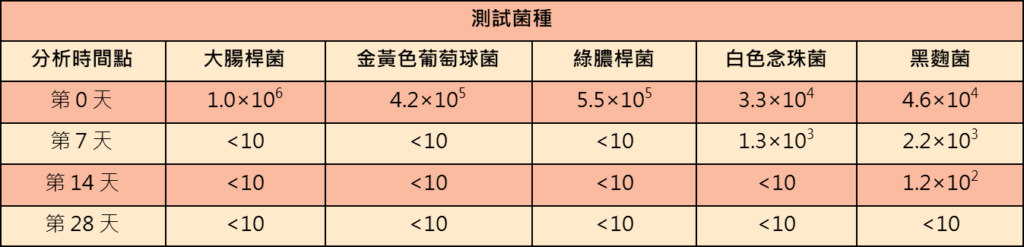
依此範例,各菌種隨時間有顯著下降,作為產品防腐效能保持作用之證明。綜合上述,業者仍可視產品風險程度決定是否執行微生物檢測與防腐效能試驗:
1. 低微生物風險產品,此類產品無須進行防腐效能試驗與微生物檢測;
2. 一次性使用產品,僅需執行微生物檢測;
3. 非上述產品,皆應進行防腐效能試驗及微生物檢測。
三、產品安定性試驗報告
一般化粧品儲存效期可能長達 3-5 年,為了確保產品在期間不會變質,因此需提供安定性試驗數據及方法。不過產品畢竟無法等 3-5 年後進行觀察才製作報告,因此可提升溫度及濕度,進行虐待試驗。依據公布之範例,即將溫度提升至 40 ℃、濕度提升至 75 % RH,針對外觀、顏色、氣味、pH、黏度、密度進行第 0、1、3、6 個月產品加速安定性試驗。確保期間沒有顯著變質,則可滿足初期階段之安定性試驗報告,不過仍需持續進行長期之常溫儲存試驗,達宣稱效期為止。
資料來源:貝爾驗證
企業好夥伴
企業問題找華宇,免費諮詢企業因為管理或是驗證上有棘手問題嗎?
企業因為員工管理或是工廠管理上有棘手問題嗎?
- 華宇服務
企業輔導與診斷、精實生產、ISO國際驗證、人才管理、戰略管理指標、組織績效、六標準差、ESG永續報告書、ESG相關輔導 - 我們將為您免費諮詢服務(請點我) 華宇官方LINE
上班時間也歡迎撥打電話諮詢 +88634951008 - 華宇免費公開班:最新企業輔導課程 (請點我)
- 化粧品 PIF 將在 2026 年全面實施,相關法規與指引
- 生物多樣性策略的全球指南-ISO 17298:2025 標準簡介(下)
- 生物多樣性策略的全球指南-ISO 17298:2025 標準簡介(上)
- 為什麼企業應該考慮進行 AA1000 永續稽核?
- IAF 近期發佈消息通知(上)-全球 ISO 標準的最新變革

